Reaksi redoks atau reaksi pengurangan dan oksidasi merupakan proses kimia dimana terjadi transfer elektron dari suatu zat ke zat lainnya dalam sebuah reaksi yang terjadi secara bersamaan. Istilah redoks sendiri merupakan singkatan dari reduction-oxidation. Suasana reaksi redoks dapat berupa suasana asam atau suasana basa. Pada kesempatan kali ini, kita akan membahas contoh soal dan jawaban penyetaraan reaksi redoks dalam suasana basa. Berikut ini adalah contoh soal dan jawabannya beserta dengan penjelasannya.
Contoh Soal dan Jawaban Penyetaraan Reaksi Redoks Suasana Basa
Berikut ini adalah contoh soal penyetaraan reaksi redoks yang terjadi dalam suasana basa:
1. Reaksi Antara Logam Mangan dan Mangan(IV) Oksida
Apa itu?
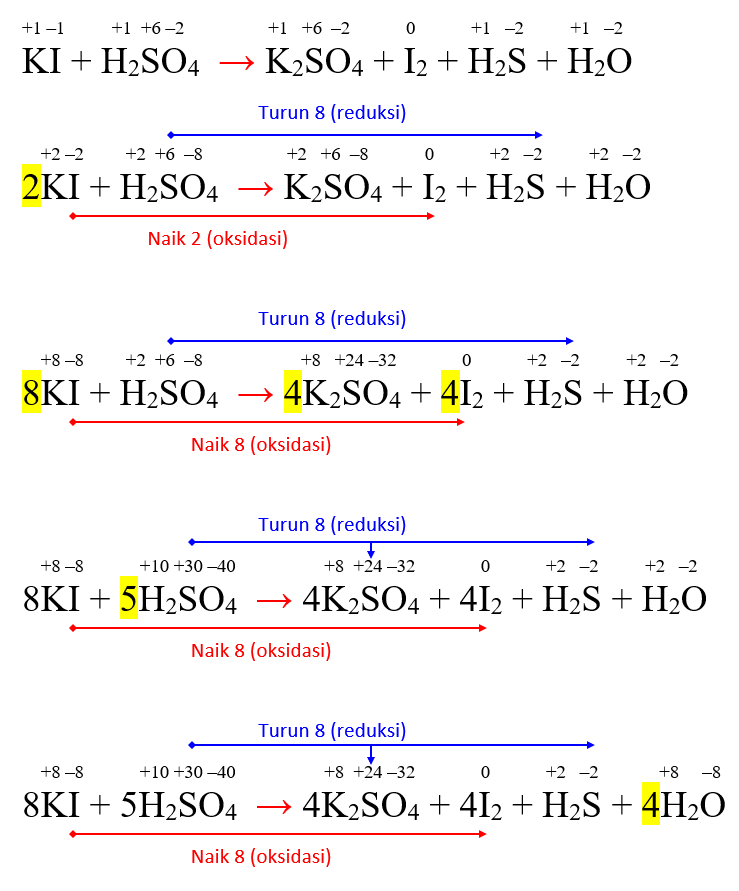
Reaksi ini merupakan reaksi antara logam mangan dengan mangan(IV) oksida dalam suasana basa.
Mengapa?
Reaksi ini terjadi karena logam mangan mengalami oksidasi menjadi mangan(II) sebagai reduktor, sedangkan mangan(IV) oksida mengalami reduksi menjadi ion mangan(II) sebagai oksidator.
Cara Penyelesaian:
Langkah-langkah penyelesaian dari reaksi redoks tersebut adalah sebagai berikut:
- Tentukan elektron yang terjadi pada setiap logam pada persamaan kimia di atas
- Ubah elektron menjadi reaksi laser
- Perhatikan aturan Konservasi Massa dan Muatan
- Jumlahkan kedua persamaan tersebut
- Jangan lupa untuk mengecek keseluruhan reaksi pada kedua sisi mengikuti prinsip konservasi massa dan muatan
- Tentukan elektron yang terjadi pada setiap zat pada persamaan kimia di atas
Jumlah elektron yang terjadi pada logam mangan(+7) dan mangan (+2) untuk membentuk ion MnO4 dan MnO2:
Mn+7+5e– → Mn+2
MnO42- + 4e– → MnO2
Dalam persamaan di atas, elektron akhir (reduktor) kebalikan dari mangan(IV) oksida, sehingga perlu dibalik persamaannya:
2Mn+7 + 5OH– → 2MnO42- + 8H2O + 5e–
Mn+2 + 4OH– → MnO2 + 2H2O + 2e–
Karena jumlah elektron pada reaktan dan produk tidak seimbang, maka perlu dikalikan dengan suatu bilangan:
10Mn+7 + 25OH– → 10MnO42- + 40H2O + 25e–
25Mn+2 + 100OH– → 25MnO2 + 50H2O + 50e–
Perhatikan bahwa bilangan elektron sama besarnya dengan 25 elektron dan harus dibalik sebagai satu kesatuan.
10MnO42- + 25Mn+2 + 30OH– → 10MnO2 + 25MnO42- + 50H2O
Bilangan massa yang direaksikan sama dengan bilangan massa yang dihasilkan, sedangkan muatan positif dan negatif seimbang pada kedua sisi persamaan.
Contoh
Penyelesaian soal di atas memberikan hasil reaksi sebagai berikut:
10MnO42- + 25Mn+2 + 30OH– → 10MnO2 + 25MnO42- + 50H2O
2. Reaksi Antara Ion Peroksidat dengan Zat Besi(II)
Apa itu?
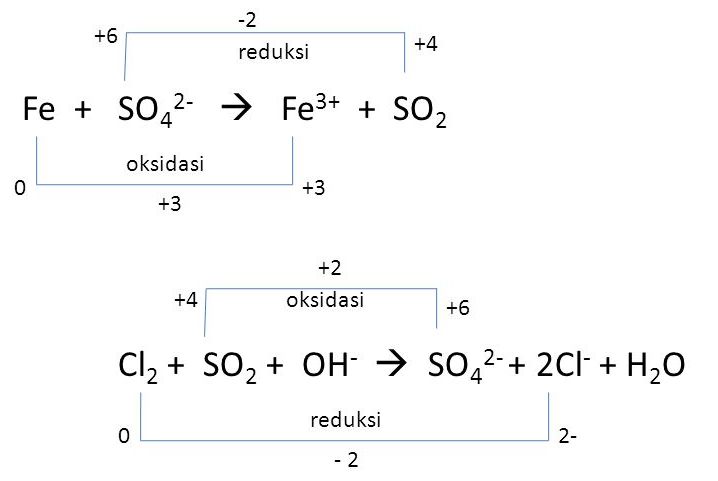
Reaksi ini merupakan reaksi antara ion peroksidat dengan zat besi(II) dalam suasana basa.
Mengapa?
Reaksi ini terjadi karena ion peroksidat, dengan rumus kimia O22-, mengalami reduksi menjadi ion oksigen dengan rumus kimia O22-, sementara zat besi(II), dengan rumus kimia Fe+2, mengalami oksidasi menjadi zat besi(III) dengan rumus kimia Fe+3.
Cara Penyelesaian:
Langkah-langkah penyelesaian dari reaksi redoks tersebut adalah sebagai berikut:
Jumlah elektron yang terjadi pada ion peroksidat dan zat besi untuk membentuk ion oksigen dan zat besi(III) adalah sebagai berikut:
O22- + 4e– → 2OH–
Fe+2 → Fe+3 + e–
Ubah elektron menjadi reaksi laser
Reaksi oksidasi perlu dibalik agar jumlah elektron sama. Jika persamaan oksidasi dibalik, maka persamaan reduksinya ikut dibalik.
2O22- + 4e– → 2OH–
Fe+2 → Fe+3 + e–
3. Kalikan persamaan untuk menyamakan jumlah elektron yang bereaksi
4O22- + 8e– → 8OH–
3Fe+2 → 3Fe+3 + 3e–
4. Jumlahkan kedua persamaan tersebut, dapat dituliskan seperti berikut
4O22- + 8Fe+2 + 12OH– → 4Fe+3 + 6H2O + 8OH–
3Fe+2 → 3Fe+3 + 3e–
5. Hilangkan ion dan molekul yang sama pada kedua sisi persamaan tersebut sehingga didapatkan persamaan akhir sebagai berikut:
4O22- + 8Fe+2 + 12OH– → 4Fe+3 + 6H2O
Contoh:
Penyelesaian soal di atas memberikan hasil reaksi sebagai berikut:
4O22- + 8Fe+2 + 12OH– → 4Fe+3 + 6H2O
Demikianlah penjelasan mengenai contoh soal dan jawaban penyetaraan reaksi redoks dalam suasana basa. Semoga bermanfaat untuk kita semua. Terima kasih.






